Inhalt
Spezifische Wärme, fühlbare Wärme und latente Wärme sind physikalische Größen:
Das spezifische Wärme eines Stoffes ist die Wärmemenge, die einer Masseeinheit dieses Stoffes zugeführt werden muss, um seine Temperatur um eine Einheit zu erhöhen. Diese Menge variiert stark in Abhängigkeit von der Temperatur, in der sich die Substanz befindet, bevor Wärme auf sie angewendet wird. Zum Beispiel benötigt man eine Kalorie, um das Wasser bei Raumtemperatur um ein Grad zu erhöhen, aber es braucht nur 0,5 Kalorien, um die Temperatur des Eises auf -5 Grad um ein Grad zu erhöhen. Die spezifische Wärme hängt auch vom atmosphärischen Druck ab. Dieselbe Substanz bei einem niedrigeren atmosphärischen Druck hat eine geringere spezifische Wärme. Die folgenden Beispiele gelten für eine Temperatur von 25 Grad und einen Druck von 1 Atmosphäre.
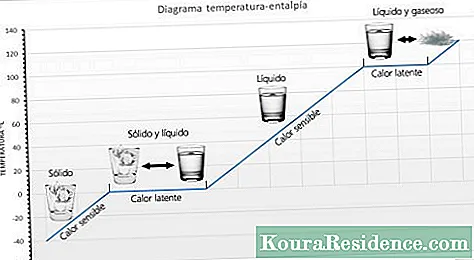
Das spürbare Hitze Es ist die Wärmemenge, die ein Körper erhalten kann, ohne seine Molekülstruktur zu beeinflussen. Wenn sich die Molekülstruktur nicht ändert, ändert sich auch der Zustand (fest, flüssig, gasförmig) nicht. Da sich die Molekülstruktur nicht ändert, wird eine Temperaturänderung beobachtet, weshalb sie als fühlbare Wärme bezeichnet wird.
Das latente Wärme Es ist die Energie (Wärme), die ein Stoff benötigt, um seine Phase (seinen Zustand) zu ändern. Wenn der Wechsel von fest zu flüssig erfolgt, spricht man von Schmelzwärme. Wenn der Wechsel von flüssig zu gasförmig erfolgt, spricht man von Verdampfungswärme. Wenn Wärme auf eine Substanz angewendet wird, die die Temperatur erreicht hat, bei der sie ihren Zustand ändert, kann die Temperatur nicht ansteigen, sondern ändert einfach ihren Zustand. Wenn beispielsweise weiterhin Wärme auf kochendes Wasser angewendet wird, wird diese niemals 100 ° C überschreiten. Latente Wärme kann je nach Stoff in der Regel in Kalorien pro Gramm oder in Kilojoule pro Kilogramm (KJ) gemessen werden.
Beispiele für spezifische Wärme
- Wasser (in flüssigem Zustand): 1 Kalorie pro Gramm, um 1 ° C zu erhöhen
- Aluminium: 0,215 Kalorien pro Gramm
- Beryllium: 0,436 Kalorien pro Gramm
- Cadmium: 0,055 Kalorien pro Gramm
- Kupfer. 0,0924 Kalorien pro Gramm
- Glycerin: 0,58 Kalorien pro Gramm
- Gold: 0,0308 Kalorien pro Gramm
- Eisen: 0,107 Kalorien pro Gramm
- Blei: 0,0305 Kalorien pro Gramm
- Silizium: 0,168 Kalorien pro Gramm
- Silber: 0,056 Kalorien pro Gramm
- Kalium: 0,019 Kalorien pro Gramm
- Toluol: 0,380 Kalorien pro Gramm
- Glas: 0,2 Kalorien pro Gramm
- Marmor: 0,21 Kalorien pro Gramm
- Holz: 0,41 Kalorien pro Gramm
- Ethylalkohol: 0,58 Kalorien pro Gramm
- Quecksilber: 0,033 Kalorien pro Gramm
- Olivenöl: 0,47 Kalorien pro Gramm
- Sand: 0,2 Kalorien pro Gramm
Beispiele für fühlbare Wärme
- Wenden Sie Wärme auf Wasser zwischen 1 und 100 ° C an
- Wenden Sie Wärme auf eine Dose an, die unter 240 ° C liegt
- Wenden Sie Blewärme an, die unter 340 ° C liegt
- Wenden Sie Wärme auf Zink an, das unter 420 ° C liegt
- Wenden Sie Wärme auf Aluminium an, das unter 620 ° C liegt
- Wenden Sie Wärme auf Bronze an, die unter 880 ° C liegt
- Wenden Sie Wärme auf Nickel an, das unter 1450 ° C liegt
Beispiele für latente Wärme
Wasser: latente Schmelzwärme: 80 Kalorien pro Gramm (es dauert 80 Kalorien, bis ein Gramm Eis bei 0 ° C zu Wasser wird), latente Verdampfungswärme: 540 Kalorien pro Gramm (540 Kalorien pro Gramm Wasser bei 100 ° C zu Dampf).
Stahl: latente Schmelzwärme: 50 Kalorien
Aluminiumoxid: latente Schmelzwärme: 85 Kalorien / 322-394 KJ; latente Verdampfungswärme: 2300 KJ.
Schwefel: latente Schmelzwärme: 38 KJ; latente Verdampfungswärme: 326 KJ.
Kobalt: latente Schmelzwärme: 243 KJ
Kupfer: latente Schmelzwärme: 43 Kalorien; latente Verdampfungswärme: 2360 KJ.
Zinn: latente Schmelzwärme: 14 Kalorien / 113 KJ
Phenol: latente Schmelzwärme: 109 KJ
Eisen: latente Schmelzwärme: 293 KJ; latente Verdampfungswärme: 2360 KJ.
Magnesium: latente Schmelzwärme: 72 Kalorien
Quecksilber: latente Schmelzwärme: 11,73 KJ; latente Verdampfungswärme: 356,7 KJ.
Nickel: latente Schmelzwärme: 58 Kalorien
Silber: latente Schmelzwärme: 109 KJ
Blei: latente Schmelzwärme: 6 Kalorien; latente Verdampfungswärme: 870 KJ.
Sauerstoff: latente Schmelzwärme: 3,3 Kalorien
Gold: latente Schmelzwärme: 67 KJ
Zink: latente Schmelzwärme: 28 Kalorien


